
 |
| |
|
|
〔概要〕(参考和訳)
CTスキャンなどの医療用放射線機器は、ほとんどの人にとって安全で効果的です。しかし、一部のX線画像診断装置と電子医療機器との間に干渉の可能性があるという問題がいくつか報告されています。
FDAは、以下に示すウェアラブル医用電子機器との電子的な干渉によって引き起こされる損傷のリスクを防ぐ方法についてrecommendationを行っている。
- ウェアラブル糖尿病デバイス
- 心臓植込み型デバイス
- 神経刺激装置
〔FDA掲載のタイトル及びURL〕
Electronic Medical Devices, X-ray Imaging and Radiation Therapy: What to Know and How to Prevent Damage | FDA
|
|
|
MRIでのマスク使用についての安全性情報(注意喚起)が、2020年12月7日付けで米国食品医薬品局(FDA)のホームページに掲載されましたので情報提供いたします。
〔概要〕
COVID-19感染拡大の中で、MRI検査中に被検者がマスクを着用している例が増えています。今回のFDAの安全性情報では、金属が含まれているマスクによる火傷の報告がされていますが、特記すべきポイントは、鼻部分の針金(ワイヤ)など目に見えて判別できるものだけでなく、抗菌コーティングに金属(銀、銅など)が含まれているものもあり、潜在的なリスクについての注意喚起がされています。
〔FDA掲載のタイトル及びURL〕
Wear Face Masks with No Metal During MRI Exams : FDA Safety Communication
https://www.fda.gov/medical-devices/safety-communications/wear-face-masks-no-metal-during-mri-exams-fda-safety-communication#:~:text=The%20FDA%20recommends%20patients%20wear,any%20metal%20during%20an%20MRI.
・FDAのMRIでのマスク使用についての安全性情報 
|
|
|
第4版の改訂発行から、薬事法が医薬品医療機器等法に改正され、法令等に合わせて、本基準を改訂し、第5版としました。内容には、特に踏み込まず、そのままを維持しています。
特に、医療機関より、「製造中止等に伴う保守部品の提供終了に関する連絡が遅い。」という指摘もあり、医機連販売・保守委員会からの自主基準の周知依頼にも合わせて対応しました。
添付文書の記載要領に係る厚生労働省通知に基づき、医療機器の品質、有効性及び安全性の確保を維持する期限を明確化するために、医療機器の「耐用期間」について、製造販売業者が使用者等へ医療機器添付文書等で情報提供することが求められ、その一助となるよう本自主基準が作成されております。会員各位におきましては医療機器の品質、有効性及び安全性の確保の推進のためにご活用願います。
・JIRA耐用期間自主基準 改訂版(第5版) 
|
|
|
|
今般、医薬品医療機器等法の施行に合わせて、平成17年(2005年)に発行した手順書を改訂しました。JIRA会員企業におかれましては、各社の実情に鑑み、手順書を改訂または作成する際、本手順書を参考にしていただければ幸いです。
・医療機器の製造販売後安全管理に係る安全管理業務(GVP)手順書 第一種製造販売業用 第2版 
|
|
|
|
【PDF版ご利用時の注意】
本PDF版は、印刷してご利用いただけますが、編集不可のセキュリティをかけております。
著作権は、JIRAに帰属します。医療機関、関連学会、団体、および当該機器の製造販売業者を除き、無断で複製、転載、頒布する等の行為を禁じます。
ここに示したチェック項目は、将来にわたり全てのリスクを示したものではありません。
※ご利用の際は、上記に同意されたものとみなしますので、ご了承ください。
|
|
MRI検査における金属物等の吸着・吸引事故、火傷及び電子情報を有するインプラント等の電子情報消失は依然として発生している状況にあります。
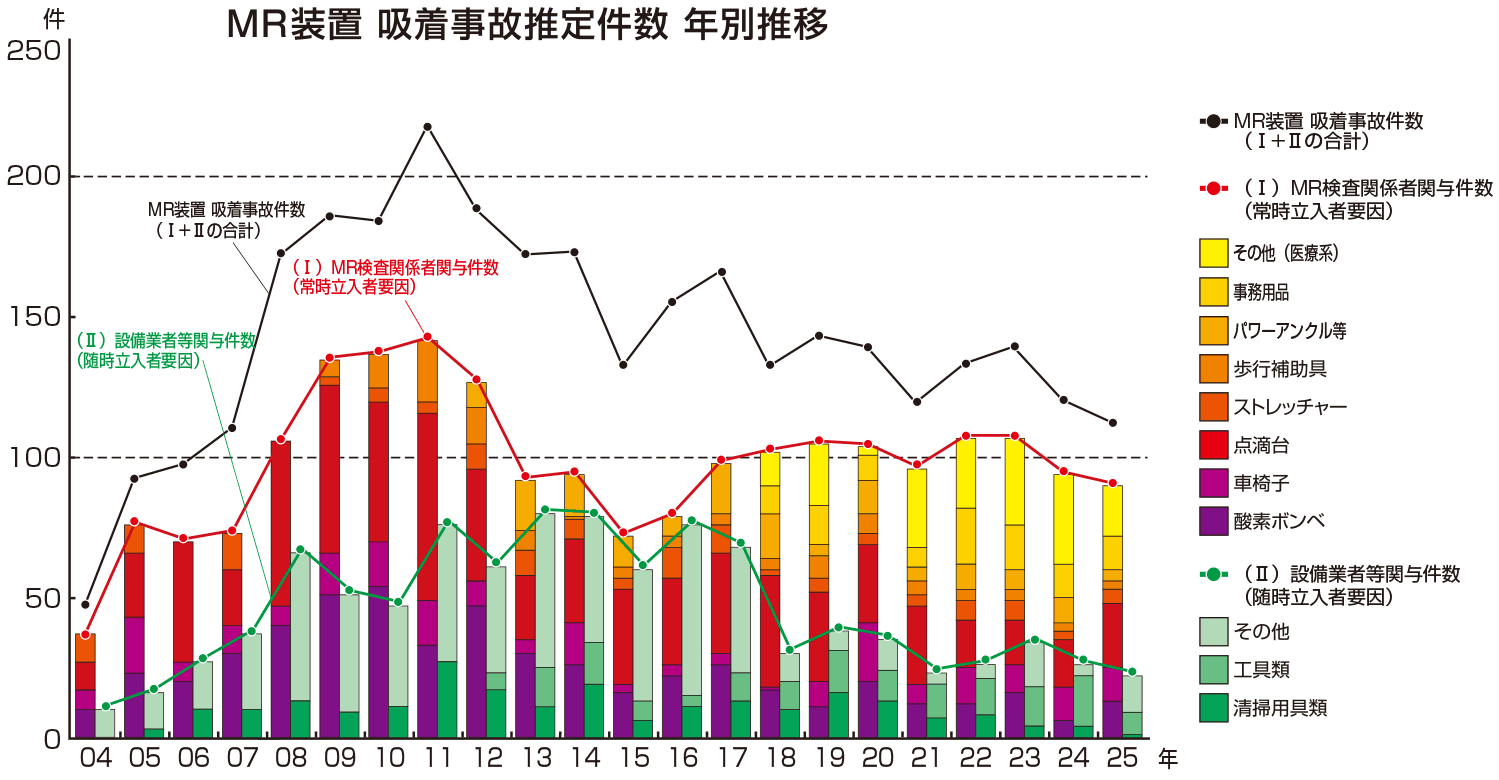
2021年10月に韓国の病院で発生した酸素ボンベの吸着によるもの、2025年7月には介助者の首に巻いた鎖による死亡事故が発生しました。特に吸着事故は、操作者、看護師または被検者等への健康被害を伴うおそれがあります。また、復旧に伴う検査機会の消失及び多額の復旧費用等の発生が考えられることから医療機関の管理者にとってもゼロ災害を目指して活動を進めていく必要があると考えております。
全体件数は2011年をピーク(約220件)に、その後、減少傾向となり、2021年は約120件程度まで減少しました。その後、一定の水準で増減していますが、2023年以降は2025年まで若干減少傾向にあります。操作者、看護師、又は被検者等への健康被害のリスクがあるため、更なる要因分析を行い、事故件数の減少に向けて活動をおこなっていきます。
JIRAではMRI装置の安全使用を呼び掛けており、日常のMRI検査時に使用していただけるチェックリストについては、医療機関の皆様に一層の注意喚起をしていただくために、新たにJIRAに寄せられたご意見や事故事例を元に留意すべき金属類・化粧品等を適宜改訂してまいります。
|
|
【販売終了】 印刷版「医療機関の皆様へ −安心・安全に医療機器をご使用していただくために(Ver.2)」
|
|
S2410-06(1)
【PDF版ご利用時の注意】
本PDF版は、印刷してご利用いただけますが、編集不可のセキュリティをかけております。
著作権は、JIRAに帰属します。医療機関、関連学会、団体、および当該機器の製造販売業者を除き、無断で複製、転載、頒布する等の行為を禁じます。
ここに示したチェック項目は、将来にわたり全てのリスクを示したものではありません。
※ご利用の際は、上記に同意されたものとみなしますので、ご了承ください。 |
|
|
医療機関の皆様へ
平成24年8月21日
一般社団法人日本画像医療システム工業会
法規・安全部会
安全性委員会
平素より工業会活動に格別のご高配を賜り、誠にありがとうございます。
2012年7月5日付けでBfArMより造影剤注入器用空シリンジに開放バイアルから造影剤又は生理食塩水を充填する際の安全衛生に関する疑念が表明されました。BfArMは、原則的に、造影剤が開放状態で環境空気と接触した場合に汚染の危険性があることを指摘しております。
下記の文章を御一読戴き、機器のご使用に際して、一層のご注意を賜りますように宜しくお願い申し上げます。
勧告原文の掲載場所:
http://www.bfarm.de/DE/Medizinprodukte/riskinfo/empfehlungen/3764-09_Kontrastmittelspritzen.html
(PDF版はこちら)
添付書類:
JIRA仮翻訳 |
|
|
http://www.info.pmda.go.jp/anzen_pmda/iryo_anzen.html
・MRI検査時の注意について(その1) ← やけど ← やけど
・MRI検査時の注意について(その2) ←金属吸着と手指の挟み込み ←金属吸着と手指の挟み込み
|
|
|
計画停電の場合におけるMR装置の準備方法について緊急発行いたしました。
・MR装置の停電時の対処方法 
|
|
|
安全性委員会では被災地で救援活動されている方々へのMR装置に係わる安全情報を提供いたしますので救援活動作業の開始前に一読頂くようお願い致します。
・安全性委員会緊急通報(MR装置)
|
|
|
昨日(3/16)「災害時エックス線撮影装置の安全な使用に関するガイドライン」の緊急配布を行いました。
本日(3/17)「災害時におけるポータブル型・移動型X線装置の安全点検チェックシート(災害時)」を緊急配布いたします。
(社)日本画像医療システム工業会安全性委員会では、平成22年度事業として、昨日配布いたしました「災害時エックス線撮影装置の安全な使用に関するガイドライン」を作成するとともに、被災地において医療機関の方々がX線装置を安全に使用するためのチェックシートをとりまとめておりました。
安全性委員会は、このチェックシートが被災地で活動されている医療機関の方々によるポータブル型または移動型のX線装置を安全に使用するための一助になればと、安全な使用に関するガイドラインとともに安全点検チェックシートを緊急措置として配布することに致しますのでご活用ください。
・災害時安全点検チェックシート 
|
|
| (※3/17 追記) |
(社)日本画像医療システム工業会安全性委員会では、平成22年度事業として、1995年(平成7年)の阪神・淡路大震災の様なライフラインが寸断され広範囲において全く機能しなくなった状況を想定した「災害時エックス線撮影装置の安全な使用に関するガイドライン」をとりまとめておりました。
今般、3月11日に日本国内観測史上最大であるM9.0の東北地方太平洋沖地震による東北関東大震災が発生し、死者および行方不明者が1万人を越えると報道されております。
医療機関の被害も伝えられている中で、負傷者数の把握も十分に行われていない状況です。
安全性委員会は、道路および交通機関が徐々に復旧するにつれ、会員企業において製品の復旧作業、消耗品等の補充のために被災地へ入ることが想定されるため、とりまとめ中のガイドラインを緊急措置として配布することにいたしました。
会員企業における従業者の安全確保および医療機関の皆様方においては対象装置の安全点検の一助になれば幸いです。
・サービス担当者への緊急・重要注意事項 
・災害時エックス線撮影装置の安全な使用に関するガイドライン 
 ・被災地で救援活動をなされている方々への重要な情報提供 ・被災地で救援活動をなされている方々への重要な情報提供 
|
|
|
(社)日本画像医療システム工業会
法規・安全部会安全性委員会
市販後安全管理専門委員会
2009年10月8日付けでFDA(米国食品医薬品局)より米国内の医療機関で発生いたしました頭部X線CTパフュージョン検査に係わる過剰被ばくの事例についての調査結果が公表されましたが、その後、事故発生場所であるカリフォルニア州では州法である「放射線管理法」基づき線量管理を義務づける追加法令が公布されました。
※CA州法1237和訳 
※Senate Bill 1237 
|
|
| 【販売は終了しました】 |
|
医療機関での管理には、医療機器の安全管理が含まれております。患者さんや使用者の安全をどの様に確保し医療機器が正しく安全に使用されているかを、毎年JIRAにて調査しています「画像診断医療機器の保守管理結果」を元にして、医療機関関係者へ保守点検の必要性をアピールするためのパンフレットを作成いたしました。
今回は、保守点検実施率が少ない一般用X線撮影装置、回診用X線撮影装置を主体に、医療機器の保守点検の必要性をアピールしております。
また、従来のA4サイズ両面刷りから見開きタイプに変更し、裏面には、これまでと同様に保守点検の必要性を説いた文言を載せております。是非とも、本パンフレットを利用して保守点検の必要性を医療機関へお伝え下さい。
申込み先 :事務局企画部(担当:高橋 TEL 03-3816-3450)
申込み方法 :メール kkkb@jira-net.or.jp
単位/価格 :100部単位/2,500円 (但し送料は別途。)
添付書類: ※パンフレット内容 
|
|
|
(社)日本画像医療システム工業会
法規・安全部会安全性委員会
市販後安全管理専門委員会
2009年10月8日付けでFDA(米国食品医薬品局)より米国内の医療機関で発生いたしました頭部X線CTパフュージョン検査に係わる過剰被ばくの事例について、12月7日付けの追加情報に引き続いて、その後の調査結果が公表されました。和訳版を仮翻訳しましたので掲載致します。
お客様におかれましては、続記のレポートをご参照頂き、機器使用に際して、なお一層のご注意を頂きますよう宜しくお願い申し上げます。
※調査結果 
※調査結果(和訳) 
以上 |
|
|
医療機関の皆様へ
平成22年10月
(社)日本画像医療システム工業会
法規・安全部会安全性委員会
市販後安全管理小委員会
平素より工業会活動に格別のご高配を賜り、誠にありがとうございます。
過日、医療機関において下記の事象が発生しました。
診断用核医学装置において、検査終了後、スライドしている天板を掴んだ患者の左手小指が寝台固定部と天板の間に挟まれ、指先を損傷した。
当工業会としては、本件のような事態の再発防止は大変重要なものと捉えておりますので、改めてご使用時の注意をお願いいたします。
ご使用の皆様におかれましては、下記の内容をご一読いただき、機器使用に際して、より一層のご注意を賜りますようよろしくお願い申し上げます。
記
画像診断装置等において、電動および手動により患者寝台および天板の上下移動・水平移動・回転、ならびにCアームなどの移動・回転の際には、次の事柄ついてのご注意をお願いいたします。
- 機器をご使用中は常に患者の状況を監視してください。(姿勢や機器との位置関係を含む)
- 機器を動作させる前には患者が安全な位置にいることを確認した上で、操作をお願いいたします。
- 次に該当する患者の場合は、特に慎重な対応をお願いいたします。
・医療従事者の指示した状態を維持できない患者
・意識のない患者
・身体に障がいのある患者
- 再度、機器の添付文書および取扱説明書を熟読していただき、ご使用ください。
ご使用中の機器をより安全にご使用いただくために、医療従事者への装置納入時と定期的な安全教育の徹底をお願いいたします。
今後ともご協力賜りますようよろしくお願い申し上げます。
※機器使用中の手指等の挟み込み防止のお願い

以上
|
|
|
(社)日本画像医療システム工業会
法規・安全部会安全性委員会
市販後安全管理小委員会
平素より工業会活動等に格別のご高配を賜り、誠にありがとうございます。 2009年12月28日付けでFDA(米国食品医薬品局)より米国内で発生いたしましたMR装置とサーモフレクト毛布(アルミはく裏打ち毛布)との相互作用についての情報が公表されました。
当工業会と致しましても、公表された内容の重要性から、MR装置をご使用の医療機関様に対して情報提供を致すことになりました。添付の文章を御一読戴き、機器のご使用に際して、一層のご注意を賜りますように宜しくお願い申し上げます。
添付書類:
- MR安全性情報

- 【対訳】FDA サーモフレクト毛布

- 【対訳】FDA 安全性リコール記事

|
|
|
(社)日本画像医療システム工業会
法規・安全部会安全性委員会
市販後安全管理小委員会
平成21年12月9日、英国医薬品庁(MHRA)より、警告文書「経直腸的に前立腺穿刺のために使用する内腔のある超音波プローブ」が発出されましたことに対して、前立腺穿刺用超音波プローブ使用についての注意喚起情報が(社)電子情報技術産業協会/JEITA 医用電子システム事業委員会ホームページにおいて公開されていますので、ご参照下さい。
http://home.jeita.or.jp/is/committee/medi-elec/index.html |
|
|
(社)日本画像医療システム工業会
法規・安全部会安全性委員会
市販後安全管理小委員会
平素より工業会活動等に格別のご高配を賜り、誠にありがとうございます。
2009年10月8日付けでFDA(米国食品医薬品局)より米国の医療機関で発生いたしました頭部X線CTパフュージョン検査に係わる過剰被ばくの事例について、公表されました。併せて、2009年12月7日付けでFDAからご使用中の全医療機関に対して、スキャン・プロトコルの管理、計画と実績線量の把握などに注意するよう追加情報が発出されました。
当工業会と致しましても、事態の重要性から、頭部X線CTパフュージョン検査の際の線量管理についての注意をお願い致すことになりました。
お客様におかれましては、続記の文章を御一読戴き、機器使用に際して、一層のご注意を賜りますように宜しくお願い申し上げます。
添付書類:
1.CT Brain Perfusion 安全性委員会からの御願い 
2.10/8付け 英文 和訳 和訳
3.12/7付け 英文 和訳 和訳
 追加情報(ご参考) 追加情報(ご参考)
4.FDA プレスリリース 2010年2月9日付け 
5.FDA 放射線放射製品 2010年2月10日付け 
6.不要な放射線被曝の低減構想へのQ&A 
7.白書 不要な放射線被曝の低減  |
|
| 【販売は終了しました】 |
診療におけるMRI装置の使用に関する重要な安全確保策の一つに磁性体吸着事故防止が挙げられます。添付文書や取扱説明書などの製品附属資料への記載を始め、ポスターや銘板など対応策が図られていますが、事故件数の減少傾向が見られないのが現状です。その中で、MRI装置における磁性体吸着事故が医療行為以外でも発生していることも見逃せません。磁性体吸着事故がもたらす様々な影響を考慮しますと、業界にとっても重要な事柄と考えられます。
このため、法規・安全部会安全性委員会および市販後安全管理小委員会では、当該製品の特徴を踏まえ医療行為以外で発生しているMRI装置における磁性体吸着事故の概要と事故防止策例を記載したパンフレットを作成しました。会員各位による顧客等への配布など、医療機関における医療機器の安全管理の啓発のためのツールとしてご活用いただくよう関係会員にご案内いたしました。
なお、安全パンフレットの追加注文を希望される場合は、以下の手続きにてお願いします。
申込み先 :事務局企画部(担当:高橋 TEL 03-3816-3450)
申込み方法 :メール kkkb@jira-net.or.jp 又はFAX 03-3818-8920
単位/価格 :100部単位/1,000円 (但し送料は別途着払いとなります。)
添付書類:
1.磁性体吸着事故防止安全パンフレット  |
|
| 【販売は終了しました】※パンフレット内容を2008年4月に差し替えました。 |
平成19年4月に医療法および医療法施行規則の一部が改正されました。これは医療における安全と信頼の確保という従来の視点に加え医療の質の向上という視点を一層重視した医療安全対策を推進するための改正施行です。今回の改正の一つに医療機器の安全確保に係る措置があり、保守点検の実施を含むため、業界にとっても重要な事柄と考えられます。このため、法規・安全部会では、JIRA製品の特徴を踏まえ医療の安全確保としての保守点検の推進を目的に法令の概要を記載したパンフレットを作成しました。会員各位の顧客等への配布するなど、医療機関における医療機器の安全管理の啓発に、また保守契約促進のためのツールとしてご活用いただくよう会員に配送いたしました。
又、本件に関して、医療機器全般に亘る安全確保の主旨で医療機器産業連合会(医機連)からも、“安心・安全にご使用して戴くために”のパンフレットが有償配布されていますので、併せてご活用いただければ幸甚です。
なお、JIRA版の安全パンフレットを追加でご注文される場合は、以下の手続きにてお願いします。
申込み先 :事務局企画部(担当:高橋 TEL 03-3816-3450)
申込み方法 :メール kkkb@jira-net.or.jp 又はFAX 03-3818-8920
単位/価格 :100部単位/1,000円 (但し送料は別途着払いとなります。)
添付書類:
1.安全パンフレット  |
|
| |
下記URLよりご参照ください。
http://www.info.pmda.go.jp/info/idx-iryouanzen.html
|
|